
השפעות התערבות "10,000 צעדים דיסלדורף" על פעילות גופנית בקרב מבוגרים החיים בקהילה
מאת: יורם אהרוני
למידע נוסף

תקציר מחקר שהתפרסם ב- PeerJ
עייפות הנגרמת מפעילות גופנית יכולה להיגרם מהפרעות במערכת העצבים המרכזית, כלומר עייפות מרכזית, או מהפרעות במערכת העצבים ההיקפית. עייפות מושרית-מאמץ היא תופעה פיזיולוגית רב-ממדית, הנובעת מהאינטראקציה המורכבת בין מערכות שונות, ובהן מערכת העצבים, מערכת השרירים והמערכת המטבולית. הוצעו תיאוריות רבות המסבירות את המנגנונים האפשריים של עייפות מושרית-מאמץ, ובהן בעיקר תיאוריית דלדול האנרגיה, תיאוריית הצטברות המטבוליטים, תיאוריית הרדיקלים החופשיים, תיאוריית הפרת ההומאוסטזיס של הסביבה הפנימית, תיאוריית שרשרת העייפות, תיאוריית חוסר האיזון במוליכים העצביים במערכת העצבים המרכזית, תיאוריית העיכוב המגן, תיאוריית המוטציה ועוד. עם זאת, המנגנון טרם הובהר במלואו. לפיכך, זיהוי והבנה של סמנים ביולוגיים של עייפות מושרית-מאמץ הפכו לחשובים יותר ויותר.
ביומרקרים הם סמנים ביוכימיים היכולים להעיד על שינויים במבנה או בתפקוד, מרמת המערכת ועד לרמת התא ואף תת-התא. הבנת משמעות הביומרקרים של עייפות מושרית-מאמץ יכולה לסייע בהערכת דרגות העייפות הנגרמת מפעילות גופנית, וכן יש לה ערך בשיקום ובטיפול לאחר המאמץ. סקירה זו נועדה לבחון באופן שיטתי את ההתקדמות המחקרית העדכנית בתחום הביומרקרים של עייפות מושרית-מאמץ, לנתח את הבסיסים הביולוגיים שלהם ולבחון את יישומיהם הקליניים הפוטנציאליים.
מאמר זה מציג סקירה של ההתקדמות העדכנית המבוססת על מחקרים בתחום הביומרקרים של עייפות מושרית-מאמץ. המאמר משלב סמנים מממדים שונים, כגון מטבוליזם של אנרגיה, מטבוליטים, מוליכים עצביים ונזקי רדיקלים חופשיים, במסגרת אחידה, במטרה להבהיר את מנגנון האינטראקציה הרב-מערכתית של עייפות מושרית-מאמץ ולספק תמיכה תיאורטית למחקר בין-תחומי. בנוסף לכך, נדונות במאמר טכנולוגיות גילוי מתקדמות, כגון חיישני מיקרו-מחטים ומטבולומיקה של רוק, המקדמות פיתוח של התקני ניטור לא-פולשניים ובזמן אמת, ומתמודדות עם מגבלות בדיקות הדם המסורתיות. המאמר מדגיש את הערך היישומי של ביומרקרים באופטימיזציה של תוכניות אימון, במניעת פציעות ספורט ובניהול עייפות כרונית. כמו כן, מוצעים במאמר כיווני פיתוח כגון שילוב רב-אומיקסי (multi-omics) סטנדרטיזציה של בדיקות והתערבות מותאמת אישית, במטרה להציג נתיבי פריצת דרך, הן לאקדמיה והן לתעשייה.
קהל היעד של מאמר זה כולל חוקרים במדעי הפעילות הגופנית, אנשי מקצוע ברפואה קלינית וברפואת ספורט, וכן מאמנים ואנשי ספורט, אשר יכולים להיחשף להתקדמות המחקרית העדכנית ולניתוח המנגנונים של סמני עייפות, ללמוד כיצד לשפר ביצועי אימון והתאוששות באמצעות תזונה מבוססת-צומח, וכיצד להתאים את עצימות האימון באמצעות ניטור לקטט בזמן אמת. בנוסף לכך, אנשי מקצוע בתעשיית המזון והתזונה יכולים להיעזר במאמר להבנת צורכי השוק ומגמות במחקר ופיתוח, ולפתח התקנים לבישים או מוצרים נוגדי-עייפות בהתבסס על מגמות טכנולוגיות עכשוויות.
המאמר מבוסס על 115 מאמרים מדעים שנמצאו בסקירה שיטתית ונכללו בו מאמרים שהתפרסמו עד אוגוסט 2025.
המנגנונים הפיזיולוגיים של עייפות מושרית-מאמץ
ניתן לסווג עייפות מושרית-מאמץ לשתי קטגוריות עיקריות: עייפות מרכזית ועייפות היקפית. עייפות מרכזית מקורה במערכת העצבים המרכזית (CNS) והיא משפיעה על יכולת המוח ליזום ולשמר פלט מוטורי. היא מאופיינת בירידה בהפעלה הרצונית של השרירים, ולעיתים קרובות קשורה לגורמים פסיכולוגיים כגון מוטיבציה ותחושת המאמץ הנתפסת. לעומת זאת, עייפות היקפית מתרחשת ברמת השריר עצמו ונובעת משינויים ביוכימיים בסיבי השריר במהלך מאמץ ממושך. עייפות זו כוללת דלדול של מקורות אנרגיה, הצטברות תוצרי לוואי מטבוליים כגון לקטט, ושינויים בריכוזי יונים המובילים לפגיעה ביכולת ההתכווצות של השריר. מחקרים הראו כי עייפות מרכזית עלולה להחמיר בעקבות עייפות מנטלית, המשפיעה על רמות המוליכים העצביים ומשנה את תפיסת המאמץ במהלך פעילות גופנית. הבנת ההבחנות הללו חיונית לפיתוח התערבויות ממוקדות להפחתת עייפות ולשיפור הביצועים הספורטיביים.
למוליכים עצביים תפקיד מרכזי בהופעה ובהתקדמות של עייפות מושרית-מאמץ. במהלך מאמץ גופני, מוליכים עצביים כגון דופמין, סרוטונין ונוראדרנלין מעורבים בוויסות מצב הרוח, המוטיבציה והתפקוד המוטורי. מחקרים מצביעים על כך שהמערכת הנוראדרנרגית, בפרט, קשורה לעייפות מרכזית, שכן עלייה ברמות הנוראדרנלין נמצאה במתאם עם תחושת מאמץ מוגברת. בנוסף לכך, סרוטונין מעורב בתגובה לעייפות, שכן שינויים ברמותיו יכולים להשפיע הן על הביצועים הגופניים והן על עייפות מנטלית. האיזון בין מוליכים עצביים אלו הוא קריטי. לדוגמה, רמות נמוכות של סרוטונין נקשרו לעייפות מוגברת ולתסמינים דיכאוניים, דבר המצביע על כך שהתערבויות המכוונות לאופטימיזציה של רמות המוליכים העצביים עשויות להפחית עייפות ולשפר ביצועים. יתרה מכך, האינטראקציה בין מערכות המוליכים העצביים מדגישה את אופייה המורכב של העייפות, הכולל היבטים פיזיולוגיים ופסיכולוגיים כאחד.
תוצרי לוואי מטבוליים, ובפרט אלה הנוצרים במהלך פעילות גופנית בעצימות גבוהה, משפיעים באופן משמעותי על תפקוד השריר ותורמים להתפתחות עייפות. הצטברות לקטט ויוני מימן מורידה את ה-PH בתוך תאי השריר, פוגעת בפעילות אנזימטית ומשבשת את ויסות הסידן, החיוני להתכווצות השריר. נוסף על כך, דלדול מאגרי הגליקוגן במהלך מאמץ ממושך עלול להגביל את זמינות האנרגיה ולהחמיר עוד יותר את העייפות. מחקרים הראו כי אסטרטגיות לשיפור ההתאוששות, כגון תיסוף פחמימות והידרציה נאותה, יכולות לצמצם את השפעתם של תוצרי הלוואי המטבוליים ולשפר את תוצאות הביצוע. הבנת המסלולים הביוכימיים המעורבים בעייפות יכולה לסייע בגיבוש תוכניות אימון ופרוטוקולי התאוששות מושכלים, ובסופו של דבר להוביל לשיפור הביצועים הספורטיביים ולהפחתת הסיכון לאימון יתר או לפציעות.
סיווג ומאפיינים של ביו-מרקרים עיקריים
חומרים הקשורים למטבוליזם של אנרגיה
הופעתה והתקדמותה של עייפות מושרית-מאמץ קשורות באופן מהותי ליכולת הגוף לייצר ולווסת אנרגיה. בהקשר זה, הדלדול, ההצטברות והזרימה המטבולית של מקורות אנרגיה מסוימים ושל תרכובות הקשורות אליהם משמשים כאינדיקטורים פיזיולוגיים מרכזיים. לפיכך, חומרים המעורבים באופן ישיר במסלולי האנרגיה התאית מהווים קטגוריה עיקרית של ביו-מרקרים להערכת עייפות.
אדנוזין טריפוספט וקריאטין פוספט
הדרישות האנרגטיות הראשוניות במהלך פעילות גופנית נענות בעיקר באמצעות דלדול מהיר של פוספגנים עתירי אנרגיה, ובראשם אדנוזין טריפוספט (ATP) וקריאטין פוספט (CP) המכונים יחד המערכת הפוספגנית. ככל שהמאמץ הגופני נמשך, הירידה במאגרי האנרגיה התוך-שריריים הללו נמצאת במתאם ישיר עם ירידה ביכולת ההתכווצות של השריר.
תרכובות פוספט עתירות אנרגיה
תרכובות פוספט עתירות אנרגיה המרכזיות למטבוליזם במאמץ כוללות אדנוזין טריפוספט (ATP) וקריאטין פוספט .(PCr) במהלך פעילות גופנית ATP מתפרק לשם שחרור אנרגיה, תוך יצירת אדנוזין דיפוספט (ADP) PCr תורם את קבוצת הפוספט שלו לצורך חידוש ATP מ-ADP. במקביל, שתי מולקולות ADP יכולות להתחבר באמצעות האנזים מיוקינאז ליצירת מולקולת ATP אחת ואדנוזין מונופוספט (AMP) תוך שחרור יוני פוספט אנאורגני .(Pi) באופן כללי, צריכת האנרגיה בפרק זמן קצר מבוססת בעיקר על קריאטין פוספט, וירידת כמותו יכולה להגיע ליותר מ־90%. תועד היטב כי אדם במשקל 70 ק״ג צורך כ-4 קילוקלוריות לדקה במהלך הליכה של שעה אחת. ככל שמשך הפעילות הגופנית מתארך, כמות הקלוריות הנצרכת עולה בהדרגה. לפיכך, ATP ו-CP והמטבוליטים הקשורים אליהם , AMP, ADP ו- Pi יכולים לשמש כאחד מהביומרקרים להערכה ראשונית של עייפות מושרית-מאמץ.
גלוקוז וגליקוגן
במהלך מאמץ עצים הנמשך מספר דקות, רוב האנרגיה מגיעה מפירוק פחמימות. לאחר פעילות ממושכת, רמות הגלוקוז בדם יורדות. עם המשך הארכת משך המאמץ, מתדלדלים במידה רבה מאגרי הגליקוגן בשריר ובכבד. בשלב זה, עד 75%–90% מגליקוגן השריר ויותר מ-90% ממאגרי גליקוגן בכבד עלולים להתרוקן. הגליקוגן אינו מצליח לשמור על רמות גלוקוז תקינות בדם, ולעיתים מתפתחת היפוגליקמיה.
שומן
עם התקדמות המאמץ, גם השומן מתחיל להיצרך. עם זאת, עייפות מושרית-מאמץ אינה מובילה לירידה משמעותית בכמות השומן הכוללת בגוף. אף על פי שתכולת השומן הכללית אינה משתנה באופן ניכר, רמות חומצות השומן והטריגליצרידים בדם עולות. מקובל להניח כי ניתן לעכב במידה מסוימת את הופעת העייפות אם אימוני סבולת משפרים את ניצול השומן במהלך המאמץ, ובכך מפחיתים את צריכת הגליקוגן ומונעים ירידה ברמות הגלוקוז בדם.
חומצות אמינו הקשורות למטבוליזם של אנרגיה
במהלך פעילות גופנית נצרכות ומנוצלות חומצות אמינו חופשיות בדם וחומצות אמינו תוך-תאיות. מבין אלו, גלוטמין, לאוצין, איזולאוצין וואלין הן חומצות האמינו הנחשבות כיום כקשורות למטבוליזם של אנרגיה. חומצות אמינו אלו נצרכות ככל שהמאמץ מתקדם, ויכולות לשמש גם כביומרקרים של עייפות מושרית-מאמץ.
מאמץ ממושך מוביל לצריכת גלוטמין ולהפחתת רמותיו בדם ובשריר. פעילות האנזימים הקשורים לגלוטמין פוחתת עקב הירידה בגליקוגן וברמות הגלוקוז.
ואלין, לאוצין ואיזולאוצין הן חומצות אמינו מסועפות .(BCAA) חומצות אמינו אלו יכולות לעבור קטבוליזם ברקמת השריר ולשמש כמקור אנרגיה. לאחר שרצי מרתון קיבלו תיסוף של חומצות אמינו מסועפות, תחושת העייפות פחתה באופן מובהק. סקירת הספרות מראה כי חומצות אמינו מסועפות מועילות במהלך מאמץ קצר ובעצימות בינונית. לאחר מאמץ הנמשך יותר מ-3 שעות או כאשר מתפתחת עייפות מושרית-מאמץ, דלדולן מציג מתאם גבוה עם מצב העייפות.
למרות שדלדול מקורות אנרגיה כגון גליקוגן ו-CP מספק הסבר הגיוני ובעל חשיבות היסטורית לעייפות, השימוש בהם כביו-מרקרים מנבאים בזמן אמת הוא מוגבל בשל מספר גורמים. ראשית, מדידה ישירה של גליקוגן תוך-שרירי היא פולשנית ואינה מעשית ברוב המסגרות הספורטיביות. שנית, קיימת שונות בין-אישית ניכרת בקצבי ניצול מקורות אנרגיה ובספי עייפות, ולכן לא קיימת רמת דלדול “אחידה” החלה על כולם. לדוגמה, ספורטאים מאומנים היטב מפגינים חסכון מוגבר בגליקוגן ויכולת חמצון שומן משופרת, מה שמעכב את הנקודה שבה דלדול גליקוגן מוביל לעייפות. לפיכך, אף שמדדים אלה חשובים מבחינה מנגנונית, מחקר עתידי צריך להתמקד בפיתוח מדדים חלופיים לא-פולשניים (למשל באמצעות ניתוח נשימה או זיעה) או במודלים מטבוליים דינמיים שיכולים לחזות את קינטיקת דלדול מקורות האנרגיה האישית, במקום להסתמך על מדידות סטטיות בדיעבד.
מטבוליטים
במהלך פעילות גופנית, מטבוליזם האנרגיה הופך לפעיל במיוחד, והגוף מייצר מגוון חומרים מטבוליים. ככל שמטבוליטים אלו מצטברים, הם תורמים לירידה ביכולת הביצוע הגופני, ובכך מובילים להופעת עייפות מושרית-מאמץ. מטבוליטים שכיחים הנצפים במהלך מאמץ כוללים לקטט, אמוניה, אוראה, גופי קטון ואחרים. מטבוליטים אלו משמשים לעיתים קרובות כביו-מרקרים להערכת עייפות מושרית-מאמץ. באופן ספציפי, בסוף תהליך הגליקוליזה נוצר פירובט. במאמץ קצר ועצים, אם אין לגוף אין מספיק חמצן, הפירובט ייהפך ללקטט. בתנאים בהם אספקת החמצן תואמת את עוצמת המאמץ, רוב הפירובט יייכנס למעגל קרבס ומהתהליך הזה ייווצר ATP כאשר החומרים שיפלטו יהיו דו תחמוצת הפחמן (CO2) ומים. אמוניה היא תוצר לוואי של מטבוליזם של חלבונים, והצטברותה עלולה להשפיע על תפקוד תקין של מערכת העצבים. אוראה היא תוצר פסולת של מטבוליזם חלבונים שיש להפריש מהגוף. נוכחות גופי קטון מעידה על שימוש בשומן כמקור אנרגיה, מצב שיכול להתרחש במהלך מאמץ ממושך או כאשר מאגרי הפחמימות מתדלדלים. מטבוליטים אלו ממלאים תפקיד מרכזי בהבנת השינויים הפיזיולוגיים המתרחשים במהלך פעילות גופנית, ובאבחון ובניטור של עייפות מושרית-מאמץ.
חומצה לקטית
במהלך פעילות גופנית עצימה, גוף האדם צורך כמויות גדולות של ATP ו-CP. כאשר מקורות אלה אינם מספקים עוד, הגוף מסתמך יותר על תהליך הגליקוליזה לאספקת אנרגיה, במאמצים מרביים הנמשכים יותר משניות בודדות. בתהליך זה מיוצר ATP מגלוקוז בתנאים אנאירוביים. בשל היעילות הנמוכה של ייצור ATP באמצעות גליקוליזה, הגוף מבצע גליקוליזה בהיקף נרחב כדי לייצר די אנרגיה, וכתוצאה מכך נוצרות כמויות גדולות של חומצה לקטית. יש לציין כי העלייה בריכוז הלקטט בדם נגרמת בעיקר מדרישות כיווץ השריר, תוך תרומה משמעותית של גיוס סיבי שריר מהירים. סיבים אלה מתאפיינים בכוח גבוה אך בעמידות נמוכה לעייפות. מצב זה גורם לכך שקצב יצירת הפירובט עולה על יכולת החמצון של המיטוכונדריה, וכך נוצר לקטט בכמות גבוהה, באופן יחסי למה שקורה בסיבי שריר איטיים. נמצא בניסויים כבר בשנות ה-80 כי עייפות מושרית-מאמץ קשורה לעלייה ברמות החומצה הלקטית לאחר מאמץ.
החומצה הלקטית עצמה אינה גורמת לעייפות; העייפות קשורה ליוני המימן (H⁺) המתפרקים מהחומצה הלקטית. הירידה ב- pH משפיעה על תהליכים רבים, כולל יכולת הטרופונין להיקשר לסידן, וכן על פעילותם של אנזימים רבים. מחקרים קודמים אישרו כי ירידת ה- pH מפחיתה את פעילותם של קינאזות כגון קריאטין קינאז,, ATPase ופוספופרוקטוקינאז (PFK) ובכך משפיעה על מטבוליזם מערכת הלקטט. מנגנון זה של ייצור לקטט, הנשלט על ידי גיוס סיבי שריר מהירים, מסביר את העלייה החדה ברמות הלקטט בדם במהלך מאמץ עצים. לפיכך, לקטט והירידה הנלווית ב- pH נותרו גם כיום ביומרקרים אמינים להערכת עייפות מושרית-מאמץ ומאמץ עד תשישות.
אמוניה
מחקרים אישרו כי במהלך פעילות גופנית ממושכת ובעצימות גבוהה, חלבונים וחומצות אמינו בגוף נצרכים ומשתתפים באספקת האנרגיה. פירוק חלבונים במהלך מאמץ ממושך מוביל ליצירת אמוניה כתוצר לוואי של פירוק חומצות אמינו. מחקרים הראו כי העלייה בריכוז האמוניה ממלאת תפקיד חשוב הן בעייפות מרכזית והן בעייפות היקפית. באופן כללי, ריכוזים גבוהים של אמוניה עלולים לפגוע בסינתזת .ATP במקביל, העלייה בריכוז האמוניה גורמת לעלייה בלחץ האוסמוטי, המביאה להפרת ההומאוסטזיס של הסביבה הפנימית. נוסף על כך, אמוניה יכולה לחדור לרקמת המוח דרך מחסום דם–מוח, להשפיע באופן טוקסי על המוח ולפגוע בתפקוד מערכת העצבים המרכזית. מחקרים עדכניים מצביעים על כך שאמוניה מעכבת את הסינתזה של ,GABA מוליך עצבי מעכב. מחסור ב- GABA מפחית את הבקרה העצבית וגורם לעייפות.
אוראה
אוראה קשורה קשר הדוק למטבוליזם של חומצות אמינו בגוף האדם, ולכן מאפשרת הערכה מקיפה יותר של התפקוד הגופני ורמות העייפות של ספורטאים. ידוע כי רמת האוראה בדם נוטה לעלות בהתאם לעומס האימון, ותהליך החזרה שלה לריכוז שהיה לפני המאמץ הוא איטי יחסית. דרגת העייפות המושרת-מאמץ נקבעת באמצעות מדידת היקף העלייה לאחר מאמץ וקצב החזרה לערכי הבסיס. כאשר רמת האוראה בדם לאחר מאמץ גבוהה ב-3 mmol/L בהשוואה לערך שלפני המאמץ, ניתן לפרש זאת כסימן לעומס אימון משמעותי המעיד על הגעה לסף העייפות.
דגימות שתן ורוק נחשבות לא פולשניות והביומרקרים שבהם יכולים לשמש לניטור עייפות בספורט. כדי לשפר את דיוק המדידות, יש להתגבר על אתגרים הקשורים לסטנדרטיזציה של עיבוד הדגימות ולקידום טכנולוגיות הזיהוי. הצעדים המרכזיים כוללים: קודם כל, סטנדרטיזציה קפדנית של תהליכי איסוף ואחסון הדגימות. בשתן, יש לבצע את הניתוח בתוך שעתיים (או עד שלוש שעות בקירור) כדי למנוע פירוק ביומרקרים. ברוק, הוספת מייצבי RNA מאפשרת שימור בטמפרטורת החדר עד שנה, ובכך מפחיתה משמעותית את הסיכון לפירוק ביומרקרים עקב הקפאה והפשרה חוזרות.
שנית, בשנים האחרונות פותחו טכנולוגיות זיהוי ברגישות גבוהה ואלה מפורטות המאמר המקורי.
התפיסה המסורתית של לקטט כתוצר פסולת הגורם לעייפות עברה שינוי עמוק. השערת “מעבורת הלקטט” מגדירה מחדש את הלקטט כנשא אנרגיה ומולקולת איתות חיונית. שינוי פרדיגמה זה מערער על מודל החמצת-היתר הפשוט, שכן הקשר בין ירידת pH לעייפות אינו תמיד ישיר או סיבתי. בדומה לכך, אף שרמות אמוניה ואוראה נמצאות בקשר עם קטבוליזם חלבונים ועייפות, המנגנוניים הספציפיים של הקשרים עדיין לא הוהברו דיים. פער מחקרי מרכזי טמון בהבנת האינטראקציה הדינמית בין מטבוליטים אלה. מחקרים עתידיים צריכים לחרוג ממדידות מתאמיות וליישם התערבויות המווסתות באופן סלקטיבי על מטבוליטים בודדים כדי לבסס סיבתיות בהתפתחות העייפות.
קינאזות ותוצרי מטבוליזם בדם
במהלך פעילות גופנית, הדם ממלא תפקיד הובלה חיוני: אספקת חמצן לצרכי האנרגיה של השריר והובלת גלוקוז חיוני. מטבוליטים כגון לקטט ואמוניה משקפים באופן ישיר את מחזור מקורות האנרגיה במהלך המאמץ. במקביל, אנזימים ומולקולות איתות במחזור הדם מספקים תובנות חשובות לגבי תגובות עקה תאיות וויסות מטבולי מערכתי בתנאי עייפות. ביומרקרים אלה, ובהם קינאזות, מתווכי חמצון-חיזור וגורמים אנדוקריניים, ממלאים תפקיד כפול: אינדיקטורים תפקודיים לכימות זרימת אנרגיה כגון חידוש כמות ATP, דינמיקת חמצן ויעילות מיטוכונדריאלית, וסימני נזק המעידים על פגיעה בשלמות הממברנה, נזק חמצוני או הפרעה הורמונלית מושרית-מאמץ. פרק זה סוקר מתווכים מרכזיים בדם שתנודותיהם מתואמות עם עייפות מושרית-מאמץ, לרבות מערכות לאגירה ולוויסות של אנרגיה, מנגנוני הובלת חמצן, מווסתי כלי דם, אנזימים מיטוכונדריאליים ואיזון היחס בין תהליכי בנייה (תהליכים אנאבולייים) ותהליכי פירוק (תהליכים קטבוליים).
קריאטין קינאז
קריאטין קינאז (CK או CPK) בסרום הוא אנזים מרכזי בתהליכים ביוכימיים, בעל יכולת לזרז יצירת ATP בעיקר באמצעות המערכת הפוספו-קריאטינית. מערכת זו ממזערת תנודות ביחס ביןATP ל-ADP במהלך פעילות עצימה כדי לשמר תפקוד התכווצותי. CK הוא אנזים המזרז התחדשות ,ATP תהליך בעל חשיבות רבה לשמירת מאזן האנרגיה בזמן המאמץ. נוכחות CK בסרום נובעת בעיקר מדליפתו מתאי השריר לדם דרך ממברנות התא. בדרך כלל רמתו בסרום נמוכה יחסית; אולם בעייפות מושרית-מאמץ עולה חדירות הממברנות ואז CK משתחרר לזרם הדם ורמתו בסרום עולה באופן ניכר.
נוסף על כך, CK מפגין תכונות נוגדות חמצון באמצעות עיכוב חמצון של ליפידים ועיכוב חמצון חלבונים במהלך מאמץ עצים. תפקיד מגן זה עשוי להפחית עייפות הנגרמת מעקה חמצונית, ומרמז על תפקיד כפול במטבוליזם אנרגטי ובהגנה תאית. במצבי עייפות חריפה, שינויים במדדים נוירו-שריריים (כגון ירידה בהספק שיא והארכת זמן כיווץ) נמצאים במתאם גבוה יותר עם ירידת ביצועים מאשר עלייה ב-CK מה שמצביע על רגישות מוגבלת של CK כביומרקר בזמן אמת בעומס קצר-טווח עד תשישות. רמות גבוהות של CK עלולות להתפרש גם כעדות להתקף לב ולכן ספורטאים המבצעים בדיקות דם שגרתיות אחרי אימון עצים וממושך, אפילו יום אחד אחריו, חייבים לציין עובדה זו בפני הבודקים כדי שתוצאות הבדיקה ינותחו כהלכה.
המוגלובין
המוגלובין, המרכיב העיקרי של תאי הדם האדומים, ממלא תפקיד מרכזי בהובלת חמצן ופחמן דו-חמצני. כאשר רמת ההמוגלובין יורדת או כאשר הדרישה לחמצן עולה, אספקת החמצן אינה מספקת, וכתוצאה מכך נפגעת יכולת הביצוע. במהלך פעילות גופנית עצימה עלולה להתרחש עייפות מושרית-מאמץ הגורמת לנזק לתאי דם אדומים, דבר המביא לשחרור המוגלובין ולירידה ברמתו מתחת לטווח התקין.
תחמוצת חנקן והאנזים nitric oxide synthase (NOS)
תחמוצת חנקן (NO) מסונתזת בגוף באופן אנזימטי מחומצת האמינו L-Arginine בעזרת האנזים nitric oxide synthase . NO ממלא תפקיד חשוב בהגברת זרימת הדם והרחבת כלי הדם, ובכך מווסת את אספקת הדם בגוף. בתחום הספורט, תיסוף ב- L-Arginine נמצא כמועיל בהפחתת פגיעות שריר ובהגברת ביצועים ובכך משפיע ישירות על היכולת האתלטית והוא גם מפחית סיכון לפציעות. לפיכך, ירידה ברמות NO עלולה לגרום לעייפות מושרית-מאמץ.
סוקצינאט דהידרוגנאז
סוקצינאט דהידרוגנאז (SDH) הוא אנזים מפתח במעגל קרבס הנקרא גם מעגל חומצת הלימון או tricarboxylic acid cycle ( (TCA ופעילותו משמשת להערכת היכולת האירובית של ספורטאים. SDH מצוי בממברנה הפנימית של המיטוכונדריה ואינו חודר לנוזל הבין-רקמתי או לדם. בעקבות נזק לרקמת השריר בשל מאמץ גופני, עולה חדירות המיטוכונדריה וכתוצאה מכך עולה תכולת SDH מחוץ למיטוכונדריה, מה שיכול לשקף את מצב מעגל ה-TCA.
טסטוסטרון/קורטיזול
טסטוסטרון הוא הורמון אנדרוגני המאיץ סינתזה של חומרים בגוף, בעוד קורטיזול הוא גלוקוקורטיקואיד המעודד קטבוליזם. יחס טסטוסטרון/קורטיזול (T/C) משמש אינדיקטור בין תהליכי הבנייה והפירוק בגוף. ריכוז טסטוסטרון חופשי יורד משמעותית בתשישות מושרית-מאמץ. עלייה בקורטיזול וברצפטורים שלו גורמת לפירוק חלבונים מעבר לקצב הסינתזה.
ביו-מרקרים מבוססי דם כגון CK והמוגלובין נמצאים בשימוש נרחב אך לעיתים קרובות מפורשים באופן שגוי. מגבלה מרכזית היא חוסר הספציפיות שלהם לעייפות. לדוגמה, רמות CK מוגברות הן מדד חזק לנזק שרירי אך אינן משקפות ישירות מצב עייפות חריפה הפוגעת בביצוע בתוך מאמץ יחיד. בדומה לכך, ירידה בהמוגלובין עשויה לנבוע מהמוליזה או משינויים במצב ההידרציה, ולא רק מירידה ביכולת נשיאת החמצן. יחס T/C אף שהוא בעל ערך להערכת איזון אנבולי–קטבולי ארוך טווח, מושפע מקצב יממתי, תזונה ועקה פסיכולוגית, ולכן פרשנותו בהקשר של עייפות חריפה היא מורכבת. לפיכך, ביומרקרים אלה מועילים ביותר כאשר הם משולבים בפאנל אינטגרטיבי ולא ככלי אבחוני בודד לעייפות. מחקר עתידי צריך להתמקד בזיהוי גורמים חדשים וספציפיים יותר בדם.
ביומרקרים הקשורים לרדיקלים חופשיים
מעבר לוויסות אנדוקריני, מאמץ עצים מעורר שרשרת תגובות חמצוניות. כאשר צריכת החמצן עולה בחדות במהלך מאמץ עצים, יש יצור יתר של reactive oxygen species .(ROS) רדיקלים אלה יוזמים תגובות שרשרת, תהליך המוביל לעקה חמצונית כאשר ייצור ה-ROS עולה על יכולת נוגדי החמצון האנדוגניים של הגוף, ביומרקרים אלה מכמתים נזק מקרומולקולרי מושרה-מאמץ ומנגנוני הגנה מפצים.
מלונדיאלדהיד
מלונדיאלדהיד (MDA) הוא תוצר פירוק של חמצון ליפידים בגוף. במידה מסוימת, ריכוזו משקף את חומרת התקפת הרדיקלים החופשיים והנזק לתאים. לאחר מאמץ עד תשישות נמצאה עלייה בתכולת MDA כתוצר מחמצון ליפידים, מה שמוכיח שניתן להשתמש בו לקביעה שמדובר במאמץ עד תשישות. ניתוח ממצאים בפלזמת הדם של רצים מיד סיום תחרות אולטרה-מרתון מצא שרמות MDA עולות משמעותית לאחר מאמץ ממושך.
סופר-אוקסיד דיסמוטאז
סופר-אוקסיד דיסמוטאז (SOD) הוא אנזים נוגד חמצון מרכזי במערכת סילוק הרדיקלים החופשיים. רמת פעילותו משקפת את עומס הרדיקלים החופשיים בגוף. בעייפות מושרית-מאמץ עם עומס רדיקלים גבוה, נדרשת פעילות SOD גבוהה. לאחר מאמץ ממושך נמצאה עלייה משמעותית ב-MDA בפלזמה ובמקביל עלייה בפעילות .SOD ניתוח יחס SOD/MDA מאפשר לשקף את קצב הייצור והסילוק של רדיקלים חופשיים, ולנתח באופן מעמיק ואובייקטיבי את השינויים במטבוליזם של רדיקלים חופשיים, ובכך להצביע על דרגת העייפות המושרת-מאמץ.
קטלאז
קטלאז (CAT) הוא אחד האנזימים המרכזיים לסילוק H₂O₂ תוך-תאי. מי חמצן (H₂O₂) הם תוצר חיזור של O₂ ובעלי תכונות חמצון חזקות, היכולות לחמצן ישירות קבוצות הידרופוביות של אנזימים ולנטרל את פעילותם. קטלאז נקשר ל- H₂O₂ ומסלק אותו. נמצא כי פעילות הקטלאז בשרירי השלד ובלב של חולדות עלתה לאחר אימון סבולת אירובי, מה שמעיד כי פעילות הקטלאז בשריר מתגברת עם התקדמות האימון. פעילות הקטלאז בגוף האדם רגישה מאוד לגירוי מאמץ: פעילות אירובית מעלה אותה משמעותית, ועלייה בעצימות האימון מגבירה אותה עוד יותר.
גלוטתיון פרוקסידאז
גלוטתיון פרוקסידאז (GSH-PX) הוא אנזים המזרז את תגובת החיזור של H₂O₂ ובכך מגן על שלמות מבנה הממברנה. רוב המחקרים מצביעים על כך שעייפות מושרית-מאמץ מובילה לעלייה בפעילות .GSH-PX מאמץ גדול גורם לעלייה משמעותית בפעילות האנזים ברקמת השריר. דווח כי בחולדות שרצו עד תשישות עלתה הפעילות של ,glutathione peroxidase glutathione S-transferase ושל glutathione reductase בכבד ובעצם, בעוד שבפלזמה פעילותם ירדה.
תפקיד העקה החמצונית בעייפות הוא נושא הנתון במחלוקת. תאוריית ‘mitohormesis’ גורסת כי ייצור מתון של ROS חיוני לאיתות הסתגלותי ולתגובות אימון. לפיכך, עלייה ב־ MDA או בפעילות אנזימים נוגדי חמצון אינה בהכרח מעידה על עייפות מזיקה. היא עשויה לשקף תהליך הסתגלות חיובי. מרבית המחקרים מודדים סמנים אלה בדם, אך רמותיהם עשויות לשקף באופן לקוי את הסביבה החמצונית בתוך סיבי השריר המתכווצים. יתרה מזו, תוצאות לא עקביות של מחקרי תיסוף נוגדי חמצון במאבק בעייפות מערערות את הנרטיב הפשטני של “מחמצנים הם רעים". מחקר עתידי צריך להתמקד במדידה ממוקדת של מצב חמצון-חיזור במדורים תאיים ספציפיים ובמהלך ההתאוששות, כדי לקבוע האם העקה החמצונית היא סיבה, מתאם או תוצאה של עייפות מושרית-מאמץ.
ביומרקרים הקשורים למוליכים עצביים מרכזיים
מחקר נרחב לאורך שנים הדגים כי מוליכים עצביים במערכת העצבים המרכזית (CNS) ממלאים תפקיד מכריע בעייפות מוטורית, ובפרט בעייפות מרכזית. מחקרים אלה קבעו כי חומרים מסוימים ובהם סרוטונין, נוראדרנלין, דופמין, אצטילכולין, חומצות אמינו ותרכובות נוספות, מעורבים באופן קריטי בתהליכי ההולכה העומדים בבסיס עייפות מושרית-מאמץ. סרוטונין מווסת מסלולים פיזיולוגיים שונים התורמים לעייפות. נוראדרנלין משפיע על תגובות עקה והוצאה אנרגטית. דופמין, שהוא בעל תפקיד מרכזי במוטיבציה ובמערכות תגמול, עלול לצאת מאיזון בהתפתחות עייפות. אצטילכולין חיוני לתקשורת עצבית-שרירית, ותפקוד לקוי שלו מוביל ישירות לעייפות שריר. נוסף על כך, חומצות אמינו ותרכובות אחרות ממלאות תפקידים ייחודיים במנגנונים המורכבים של עייפות במאמץ.
הידרוקסיטריפטמין
הידרוקסיטריפטמין (5-HT) הוא מטבוליט של טריפטופן ומוליך עצבי מרכזי ב-CNS. טריפטופן הוא הסובסטרט ליצירת וזמינותו משפיעה על קצב התהליך. טריפטופן חופשי בפלזמה יכול לחצות את מחסום דם–מוח ולהשפיע על רמות הידרוקסיטריפטמין .במהלך מאמץ מתגברת הליפוליזה (פירוק ליפידים), רמות חומצות השומן החופשיות עולות, ובהתאמה עולה הטריפטופן החופשי, מה שמגביר את סינתזת הידרוקסיטריפטמין במוח. מחקרים הראו כי מאמץ מעלה את רמות הידרוקסיטריפטמין במערכת המרכזית, ועלייה זו קשורה להתפתחות עייפות מרכזית. הוצע כי הידרוקסיטריפטמין עשוי להיות מווסת של עייפות מרכזית. הוא פועל כמוליך עצבי מעכב המפחית את הדחף מהמרכז לפריפריה ובכך מפחית את כושר הביצוע. מחקרים מצאו גם כי עם הארכת משך המאמץ פוחתת היכולת האנאבולית של הידרוקסיטריפטמין, דופמין וחומרים אחרים במוח.
דופמין
דופמין מווסת את דרגת המתח של רקמת השריר, והוא המוליך העצבי הראשון שנמצא שהוא בעל תפקיד משמעותי בעייפות מושרית-מאמץ. בדרך כלל, מטבוליזם הדופמין עולה במוח לאחר מאמץ. נמצאו שתי סיבות עיקריות לעלייה בדופמין במוח לאחר תחילת המאמץ: הגברת סינתזת הדופמין והגברת הקישור לרצפטורים שלו. עם זאת, מחקרים הראו כי סינתזת הדופמין במוח האמצעי של חולדות נחלשת בעייפות מרכזית, וכי רמות דופמין גבוהות יכולות לעכב את התפתחות העייפות. ממצאים אלה מצביעים על כך שבעייפות מושרית-מאמץ רמות הדופמין במוח יורדות.
נוראדרנלין
נוראדרנלין (NE) הוא מוליך עצבי המסונתז ומופרש מקצות עצבים מפרישי אדרנלין. הוא מיוצר מדופמין באמצעות האנזים דופמין β-הידרוקסילאז. מחקרים אישרו כי נוראדרנלין בהיפותלמוס יורד לאחר מאמץ ותשישות, וכי תכולתו משפיעה על רמת המטבוליזם של NE ושניהם יכולים לעכב את פעילות ההיפותלמוס, אחד הגורמים לעייפות מושרית-מאמץ.
אצטילכולין
אצטילכולין (ACh) הוא מוליך עצבי המשתחרר ב- CNS מקצות עצבים מפרישי אצטילכולין. הסינתזה שלו והפרשתו חיוניות לפעילות תקינה של מערכת העצבים המרכזית. קצב סינתזת ACh מושפע מהקדם-חומר כולין. לאחר ריצת מרתון, רמת הכולין בפלזמה יורדת בכ־40%, ותיסוף משקאות כולין לשמירת רמותיו בפלזמה מעכב את הופעת העייפות. תיסוף כולין במהלך מרתונים יכול אפוא לדחות את העייפות.
חומצות אמינו (בקשר למוליכים עצביים)
נכון להיום, חומצות האמינו שנקשרו במחקרים לעייפות מרכזית כוללות בעיקר ,GABA חומצה גלוטמית ,(Glu) וחומצות אמינו מסועפות – (BCAA) איזולאוצין, לאוצין וואלין. החומצות המסועפות חשובות לאספקת אנרגיה, והוצע כי יש להן תפקיד בהתפתחות עייפות.
GABA הוא מוליך עצבי מעכב. אחת הסיבות לעייפות מוטורית מרכזית היא עלייה ברמות . .GABA עם הארכת משך המאמץ הגוף ייראה כמו במצב של היפוקסיה (מחסור בחמצן): תהליך חמצון GABA נחלש וריכוזים גבוהים של GABA גורמים לעיכוב פוסט-סינפטי. רמות גבוהות של GABA במוח עלולות להוביל לעייפות מושרית-מאמץ.
גלוטמט הוא מוליך עצבי מעורר מרכזי ב- CNS המצוי בשפע במוח. רמות תקינות שלו חיוניות לשמירה על עוררות עצבית, והוא המוליך של רוב הסינפסות המעוררות. כאשר רמות הגלוטמט במוח משתנות באופן חריג, תפקוד המערכת המרכזית נפגע וזה אחד הגורמים לעייפות מושרית-מאמץ.
NO ו-NOS ואנדותלין
תחמוצת החנקן (NO) משפיעה על הרחבת כלי הדם ומשמשת גם כמוליך עצבי חשוב. היא בעלת תפקיד פיזיולוגי משמעותי במאמץ, במיוחד במערכת הקרדיווסקולרית. NO מתבטא בתאי רקמה כמולקולת איתות תוך-תאית, הגורמת להרפיית שרירים חלקים בכלי הדם באמצעות אינטראקציה עם .cGMP מחקרים אישרו כי nitric oxide synthase (NOS) פעיל באופן תקין ברקמת המוח, אך ביטויו נחלש משמעותית לאחר עומסי אימונים כבדים, ממצא המעיד שעייפות מפחיתה ביטוי NOS במוח.
אנדותלין (ET) הוא פוליפפטיד קטן ופעיל המעודד כיווץ כלי דם, והוא החומר היעיל ביותר לכיווץ כלי דם, ופעילות מנוגדת לזו של .NO מחקרים קודמים הראו כי מאמץ מגביר את ביטוי ET ברקמות, גורם לכיווץ כלי דם ולבסוף להיפוקסיה. רמות ET נמצאות במתאם גבוה עם עצימות המאמץ, ועייפות מושרית-מאמץ מתרחשת עקב איסכמיה (הפרעה בזרימת הדם) והיפוקסיה (מחסור בחמצן) כאשר עומס האימון גבוה מדי.
מגבלה מרכזית בתחום זה היא הסתמכות יתר על מדדים פריפריים להסקה על שינויים במוליכים עצביים מרכזיים. מאחר שמחסום דם–מוח מגביל מעבר חופשי של מולקולות בין הפריפריה למוח, הסקות כאלה הן ספקולטיביות במידה רבה. "השערת העייפות המרכזית” הקלאסית, שהתמקדה בעבר ב- הידרוקסיטריפטמין, מאותגרת כיום: דופמין ונוראדרנלין נחשבים חשובים באותה מידה בוויסות מוטיבציה ותפיסת מאמץ. מגבלות מתודולוגיות מהוות אתגר נוסף: בעוד שמחקרי בעלי חיים מאפשרים מדידות מוח ישירות, מחקרים בבני אדם נשענים על מדדים עקיפים. אינטראקציות בין מטבוליטים פריפריים להעברה עצבית מרכזית מהוות חזית מחקרית מבטיחה שעדיין לא נחקרה דיה.
ביומרקרים בשתן
באמצעות מדידה מדוקדקת של ריכוז מטבוליטים בשתן באמצעות טכניקות אנליטיות מתקדמות, ניתן לשקף בעקיפין את השינויים המטבוליים המתרחשים בגוף, וכך להסיק על דרגת העייפות המושרת-מאמץ. ניתוח מטבוליטים בשתן מספק תובנות חשובות לגבי תגובת הגוף למאמץ גופני ומסייע להבנת המנגנונים העומדים בבסיס עייפות מושרית-מאמץ. יתרה מכך, בדיקות שתן הן בעלות חשיבות רבה בהערכה קלינית וספורטיבית, והביומרקרים בשתן מהווים אחד האינדיקטורים האמינים לזיהוי עייפות מושרית-מאמץ.
טבלה 1:
סמנים ביולוגיים הקשורים לעייפות בעקבות פעילות גופנית בבדיקות שתן שגרתיות.
| ביו-מרקר | גורם משפיע | מצב תקין | מצב אחרי מאמץ |
|---|---|---|---|
| pH בשתן | חומצה לקטית, פירובט ועוד | pH ≈ 7 | |
| ירידה של 3–4 יחידות pH | |||
| חלבון בשתן | סינון גלומרולרי בכליה | כמות זעירה: 2–8 מ״ג | עלייה פי 3–4 |
| דם סמוי בשתן | סינון תאי דם אדומים | לא ניתן לזיהוי | ניתן לזיהוי |
| בילירובין | פירוק המוגלובין | ערך תקין | עלייה בריכוז |
| אורובילינוגן | פירוק המוגלובין | ערך תקין | עלייה בריכוז |
| קריאטינין בשתן | פירוק קריאטין או קריאטין-פוספט | ערך תקין | עלייה בריכוז |
רוק
הרוק הוא מדד נוח מאוד לאיסוף, בטוח לחלוטין ולא פולשני. בשנים האחרונות המחקר על השימוש ברוק להערכת מצב גופני במהלך פעילות גופנית זוכה לעניין הולך וגדל, במיוחד בתחום הספורט. עבור ספורטאים, האפשרות להשתמש ברוק במקום בדם או בשתן להערכת מצב גופני מציעה גישה מהירה ונוחה משמעותית. הפוטנציאל של הרוק כמקור לסמנים ביולוגיים להערכת שינויים פיזיולוגיים הנגרמים על ידי פעילות גופנית נבדק במספר רב של מחקרים. איסוף הרוק אינו פולשני, והוא מתקבל ביתר קלות על ידי ספורטאים, מה שמפחית את אי הנוחות והסיכונים הפוטנציאליים הכרוכים בשיטות מסורתיות. יתר על כן, ניתוח הרוק יכול לספק תובנות חשובות לגבי היבטים שונים של מצב גופני, כגון רמות הורמונים, תפקוד חיסוני ועקה חמצונית. תחום מחקר מתפתח זה מציג פוטנציאל רב לשיפור ניטור וניהול הבריאות והביצועים של ספורטאים. בעתיד, צפויים פיתוחים נוספים במחקר סמני ביולוגיים ברוק, שיאפשרו הערכות מדויקות ומקיפות יותר של תגובת הגוף לפעילות גופנית, ובכך יסייעו לספורטאים ומאמנים לקבל החלטות מושכלות יותר לגבי אימון ותחרות.
חומציות הרוק
עקב עלייה בייצור חומצת חלב לאחר פעילות גופנית מאומצת לאורך זמן, כמות ה-CO2 בדם עולה, וחומרים חומציים כגון גופי קטון ופירובט מצטברים, מה שמוביל לירידה בערך ה-pH של הדם ולפיכך גם לירידה ב- pH של הרוק. כאשר מתרחשת עייפות כתוצאה מפעילות גופנית, לעיתים מופיעה חומציות יתר (acidosis) שיכולה להפחית את יכולת השרירים לבצע פעילות גופנית ולגרום גם לתסמיני עייפות של מערכת העצבים המרכזית. יש לצרוך חומרים אלקליניים בכמות מספקת לאחר פעילות גופנית.
אימונוגלובולין A ברוק
רמת אימונוגלובולין (SIgA) A ברוק היא אחד המדדים החשובים למצב החיסוני של האדם. לאחר פעילות גופנית אינטנסיבית או ממושכת, הדיכוי החיסוני הנגרם על ידי הפעילות הגופנית מוביל לירידה ברמת אימונוגלובולין. A רוב המחקרים מצביעים על כך שרמת SIgA יכולה לשמש כאינדיקטור להערכת עומס אימון, שכן היא יורדת לאחר תקופות קצרות של פעילות אינטנסיבית ומתישה. לדוגמה, במחקר אחד ביצעו 26 נשים פעילות של שלושה קטעים של דיווש מרבי על אופניים למשך 30 שניות עם 3 דקות הפסקה ביניהם. נמצאה אצלן ירידה זמנית ברמות אימונוגלובולין A ברוק. לסיכום, אימונוגלובולין A ברוק הוא סממן ביולוגי חשוב להערכת עייפות כתוצאה מפעילות גופנית.
רכיבים נוספים ברוק ששימשו כסמנים ביולוגיים
עם פיתוח טכנולוגיות High-throughput ויישומן בספורט, זוהו יותר רכיבים ברוק, שיכולים להחליף בדיקות דם מסוימות. רכיבים אלה משמשים גם כסמנים לפעילות גופנית. חוקרים השתמשו בדם וברוק של ספורטאים לפני פעילות גופנית ואחריה ומצאו ברוק סמנים ביוכימיים הקשורים לספורט. זוהו קבוצת חלבונים קטנים (sMW) ברוק לאחר פעילות גופנית ונמצא מתאם חיובי בין חלבונים קטנים לעייפות הנגרמת על ידי פעילות גופנית.
מגבלות במדדים לא פולשניים
העניין בסמנים ביולוגיים לא פולשניים צריך להיות מלווה במודעות למגבלות האנליטיות והטרום-אנליטיות שלהם. מצב ההידרציה (כמות המים בגוף) משפיע משמעותית על ריכוז החומרים בשתן, מה שמחייב תיקון לפי קריאטינין ופרוטוקולים מחמירים לאיסוף דגימות. באופן דומה, מדידות הורמונים ברוק כגון קורטיזול ו- IgA רגישות מאוד למחזור היומי, טכניקות האיסוף ומצב בריאות הפה. מגבלה מרכזית היא שרבים מהמחקרים מדווחים על שינויים בסמנים אלה מבלי לתקף תחילה טווחי התייחסות מאומתים לאוכלוסיות ספציפיות בתנאי פעילות גופנית. לכן, בעוד שסמנים ביולוגיים לא פולשניים מתאימים לניטור לאורך זמן, השימוש הנוכחי שלהם לאבחון חד-פעמי או במחקרי רוחב על עייפות הוא מוגבל. הכיוון העתידי הוא פיתוח מערכות חיישנים משולבות למדידה בזמן אמת, בשילוב עם שיטות למידת מכונה לפירוש הנתונים הרב-פרמטריים המורכבים שהם מייצרים.
שיטות זיהוי סמנים ביולוגיים
פיתוח טכנולוגיות בדיקות דם
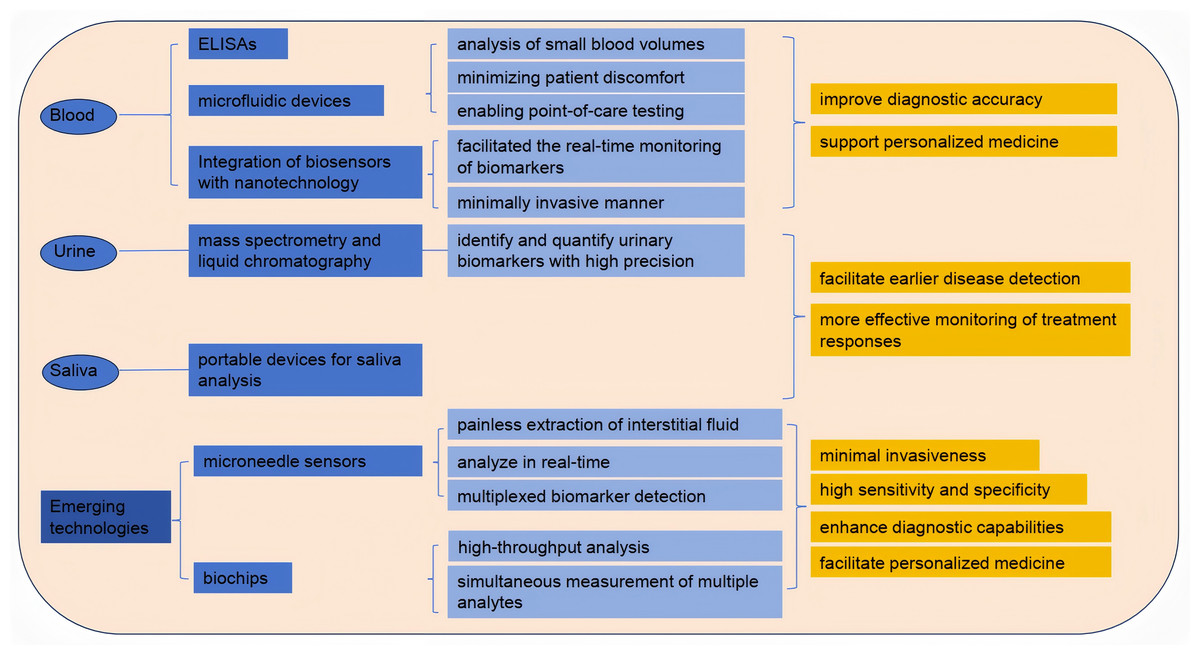
התפתחות טכנולוגיות בדיקות הדם שיפרה משמעותית את הגילוי והניטור של סמנים ביולוגיים למחלות שונות. שיטות מסורתיות, כגון ELISA ובדיקות דם שגרתיות, סללו את הדרך לטכניקות מתקדמות יותר. בדיקות דם שגרתיות משמשות לא רק בפרקטיקה קלינית אלא גם להערכת מצב ספורטאי, ומספקות הבנה מעמיקה יותר של הקשרים בין סמנים ביולוגיים בדם, ביצועי אימון ועייפות הנגרמת מפעילות גופנית. חידושים אחרונים כוללים מכשירי Microfluidics שמאפשרים ניתוח כמויות קטנות של דם, מקטינים את אי הנוחות ומאפשרים בדיקות במקום .שילוב חיישנים ביולוגיים עם ננוטכנולוגיה מאפשר ניטור בזמן אמת של סמנים כמו גלוקוז וחומצת חלב, עם פולשנות מינימלית.
ניתוח סמנים ביולוגיים בשתן וברוק
שתן ורוק הפכו לנוזלים ביולוגיים חשובים לניתוח סמנים ביולוגיים, עם יתרונות משמעותיים על פני דגימות דם מסורתיות. שתן נוח במיוחד לאיסוף ומכיל מגוון רחב של סמנים המצביעים על מחלות שונות, כולל תפקוד כלייתי והפרעות מטבוליות. מחקרים עדכניים השתמשו בטכניקות מתקדמות כגון ספקטרומטריית מסה וכרומטוגרפיית נוזלים לזיהוי וכימות סמנים בשתן בדיוק גבוה. באופן דומה, רוק זוכה לתשומת לב בשל היכולת שלו לשקף את הבריאות הכללית, כאשר מחקרים רבים מצביעים על סמנים הקשורים לבריאות הפה, מחלות מערכתיות ואפילו סרטן .פיתוח מכשירים ניידים לניתוח רוק, בשילוב עם התקדמות במחקר פעילות חלבונים ומטבוליזם, הגדילו את היתכנות השימוש ברוק ככלי אבחוני
טכנולוגיות מתקדמות: חיישני Microneedle וביוצ’יפים
חיישני Microneedle וביוצ’יפים מייצגים את החזית של טכנולוגיות גילוי סמנים ביולוגיים, בשילוב פולשנות מינימלית עם רגישות וספציפיות גבוהה. Microneedles מאפשרות שאיבת נוזל בין-תאי ללא כאב, שניתן לנתחו עבור סמנים כמו גלוקוז, חומצת חלב ואלקטרוליטים בזמן אמת. פיתוחים אחרונים כוללים פלטפורמות ביו-סנסור משולבות עם גילוי מרובה סמנים, המאפשר ניטור כולל של מצב בריאותי .בנוסף לכך, ביו-צ’יפים מאפשרים ניתוח High-throughput ומדידה סימולטנית של מספר רב של חומרים. טכנולוגיות אלה משפרות את יכולות האבחון ומאפשרות רפואה מותאמת אישית באמצעות ניטור רציף של סמנים במצבים פיזיולוגיים שונים.
שימוש בטכנולוגיות Multi-omics במחקר עייפות הנגרמת מפעילות גופנית
טכנולוגיות Multi-omics חוללו מהפכה בהבנת עייפות הנגרמת מפעילות גופנית על ידי שילוב סוגי נתונים ביולוגיים שונים, כולל גנומיקה (חקר החומר התורשתי), פרוטאומיקה (חקר החלבונים), מטבולומיקה (חקר חילוף החומרים) וטרנסקריפטומיקה (חקר RNA). טכנולוגיות אלה מאפשרות לראות תמונה כוללת של מעורבות המנגנונים המולקולריים האלה בתופעת העייפות במהלך הפעילות הגופנית ואחריה. לדוגמה, שילוב נתוני טרנסקריפטומיקה עם פרופילים מטבוליים מסייע להבין את מסלולי המטבוליזם המשתנים בעייפות, ומספק תובנות לגבי ניצול תת-חומרים אנרגטיים בשריר.
סטנדרטיזציה ויישומים קליניים של סמנים ביולוגיים
השימוש הקליני בסמנים ביולוגיים לעייפות הנגרמת על ידי פעילות גופנית מוגבל עקב חוסר סטנדרטיזציה במדידה ובפירוש. סמנים כגון רמות לקטט, השונות בדופק (heart rate variability) ופרופילי ציטוקינים, יש להם פוטנציאל מבטיח, אך שימושם הקליני מוגבל עקב שונות בשיטות הבדיקה ובאוכלוסיות הנבדקות. פיתוח פרוטוקולים סטנדרטיים כולל כל היבטי ההערכה חיוני לשילובם בפרקטיקה קלינית.
שונות אישית בסמנים ביולוגיים של עייפות
הבנת ההבדלים האישיים בעייפות חיונית לפיתוח גישות מותאמות אישית לאימון והתאוששות. מחקרים עדכניים מדגישים שונות משמעותית בסבילות השרירים לעייפות ובקצב ההתאוששות בין אנשים, המושפעת מגורמים גנטיים, פיזיולוגיים ופסיכולוגיים. שימוש בסולם (Rating of Perceived Exertion) RPE הוא כלי פרקטי ומבוסס מדעית להערכת מצב העייפות של אדם בזמן אמת.
מסקנות ומבט לעתיד
סקירה זו הביאה את ההבנות הנוכחיות על סמנים ביולוגיים הקשורים לעייפות הנגרמת על ידי פעילות גופנית, כולל תת-חומרים אנרגטיים, תוצרי מטבוליזם, אינדיקטורים ביוכימיים בדם, פרמטרים של עקה חמצונית, נוירוטרנסמיטרים וסמנים לא פולשניים. למרות שהסמנים מספקים תובנה למורכבות העייפות, התחום מוגבל על ידי ממצאים מתאמיים ושברים בידע.
סמנים קלאסיים כגון לקטט, אמוניה, קריאטין קינאז וקורטיזול נתמכים במחקרים רבים, אך פרשנותם מורכבת עקב חוסר ספציפיות ושונות גבוהה בהקשר. סמנים לא פולשניים ברוק ובשתן מציעים אפשרויות מעקב בזמן אמת, אך שימושם מוגבל עקב חוסר סטנדרטיזציה. טכנולוגיות חדשות כמו חיישני Microneedle ופלטפורמות Multi-omics מראות פוטנציאל רב, אך יש צורך בשיפורים מתודולוגיים ושילוב ניתוחי נתונים.
המחקר העתידי צריך למקד את עצמו בהבנת הדינמיקה הזמנית והקשרים הסיבתיים של השינויים בסמנים, תוך שימוש במחקרי התערבות ובמודלים חישוביים מתקדמים. יש צורך בשילוב בין מדידות מעבדתיות לכלי ניטור בשטח, תוך התחשבות בשונות אישית בערכי בסיס ותגובת סמנים. בנוסף לכך, שילוב אינדיקטורים פיזיולוגיים עם היבטים תפיסתיים וקוגניטיביים של עייפות חיוני לפיתוח מסגרות הערכה רב-ממדיות ומקיפות.
לסיכום, התקדמות המחקר בעייפות הנגרמת מפעילות גופנית תלוי בגישות אינטגרטיביות המשלבות מערכות סמנים רב-ממדיות, טכנולוגיות מתקדמות ועקרונות רפואה מותאמת אישית, ובכך משפרות ניטור, הפחתת העייפות והניהול שלה, כדי לשפר ביצועים ספורטיביים ולשמור על בריאות הספורטאים והאוכלוסייה הכללית.
Liu X, Liu J. 2026. Research progress on exercise fatigue from the perspective of fatigue biomarkers. PeerJ 14:e20424
יש לך שאלה למומחים של המרכז האקדמי לוינסקי-וינגייט? אין צורך להתבייש, רק ללחוץ כאן